3D打印最新Science!斯坦福大学!
3D打印技术参考注意到,2025年3D打印技术领域第6篇Science文章于6月12日发表。来自斯坦福大学发表了题为“Rapid model- guided design of organ- scale synthetic vasculature for biomanufacturing”的文章。Science同期发表了来自剑桥大学的华人学者黄艳燕教授以及悉尼大学的华人学者居理宁教授联名评论文章“Synthesizing vascular trees at speed”。
这项研究主要探讨了生物组织领域的重大进展,聚焦使用3D打印技术快速开发具有人体器官尺度的大尺寸血管网络。研究人员开发了一个模型驱动的设计平台,能够使血管的生成速度提升230倍;结合多保真计算流体动力学模拟和三维生物打印,最终使制造出的血管模型结构、形状及尺寸均能达到人体器官规模。该研究将为体外构建具有活体功能的器官来用于药物筛选、疾病研究和移植带来新的发展契机。
 https://www.science.org/doi/10.1126/science.adj6152
https://www.science.org/doi/10.1126/science.adj6152

血管化——生物制造的核心挑战
随着生物打印方法已能够精确放置细胞且保持良好的活力,目标已转向生成人体尺度、生理相关的组织。在人工组织中再现血流动力学对于其存活至关重要。真实的组织器官中细胞与血管的距离不超过100μm;在代谢需求高的组织中,这个距离可能小于20μm,血管密度可能超过每毫米2500个血管。

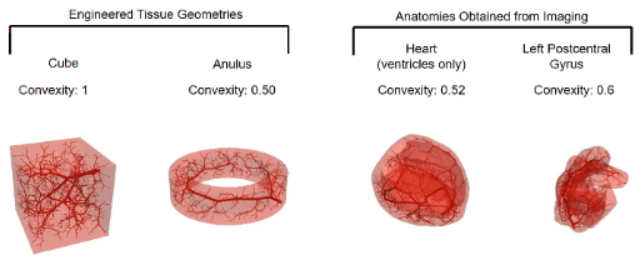 在立方体和双心室中设计的传统晶格血管网络和合成血管网络
在立方体和双心室中设计的传统晶格血管网络和合成血管网络
血管为细胞提供营养、输送氧气并清除代谢废物。因此,在体外构建组织器官的一个重要工作就涉及到构建出通道来实现血管的功能,并会以灌注的形式向该组织器官模型中输入必要的生物、测试等物质。
然而,构建如此复杂血管网络的难度显而易见。要构建血管网络,首先应获取它的具体分布、再构建模型,然后再进行制造。目前,第一步的实现也非顺利,传统上建立复杂的模型通常需要几天时间。当前获取真实组织中血管分布的方法有从图像数据中分割血管以及通过冷冻显微镜和光学切片显微镜技术分割血管。前者的问题在于分辨率不足,后者的问题在于很少有直接的解剖学对应物可供提取成像,且仍然存在数据量巨大、三维重建困难、分辨率问题等。
 具有1000个终端的血管树分别位于立方体、环形、双心室和脑回组织域中
具有1000个终端的血管树分别位于立方体、环形、双心室和脑回组织域中
现代灌注设计依赖简单晶格结构,无法很好地再现天然血管的拓扑结构和血流动力学。这些理想化的设计在低细胞密度组织中尚能发挥作用,但它们无法满足临床细胞密度下的组织代谢需求,导致所构建的人体尺度组织器官在体外的存活率很低。
血管网络设计速度提升230多倍
斯坦福大学的研究团队介绍了一种合成血管工具,能够在几分钟内生成跨器官的树网络模型,通过结合血流动力学模拟和3D打印技术,能够自动化的完成血管管道构建。
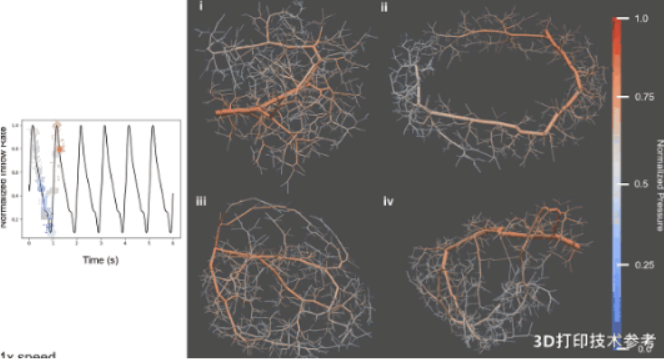
为了能够快速建模器官尺度的合成血管系统,研究人员采用四种不同的算法——将复杂问题分解为较小的子问题来求解;在每次添加血管时临时存储中间结构来减少计算复杂性;部分隐式体积表示法将3D体积切分为更小的部分,能够高效处理非凸几何体,如血管分支和心脏瓣膜,而无需使用计算成本高昂的网格;分层碰撞检测使用树结构来图形模拟和筛选两个血管之间的潜在交点。多目标优化同时做出决策,来生成闭合循环的血管回路。
为展示该平台的设计能力,研究人员计算生成了非凸形双心和环形几何结构中具有10^4到10^6个终端血管的合成血管。当达到100万个出口时,血管直径从1.2毫米到5微米不等,符合新生儿冠状动脉的形态计量数据。每百万血管树的生成大约需要5小时,从组织间隙到最近的血管的平均距离测量约为180到190微米。若纳入促血管生成方法,能够通过引入毛细血管网络进一步降低该平均距离。
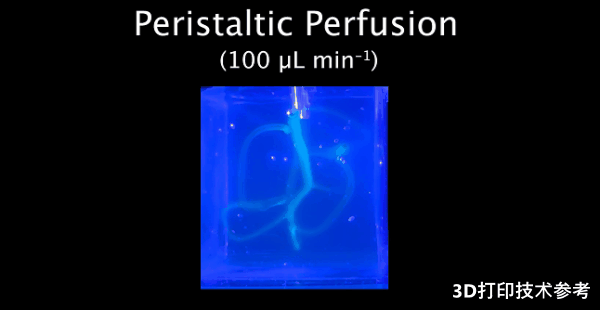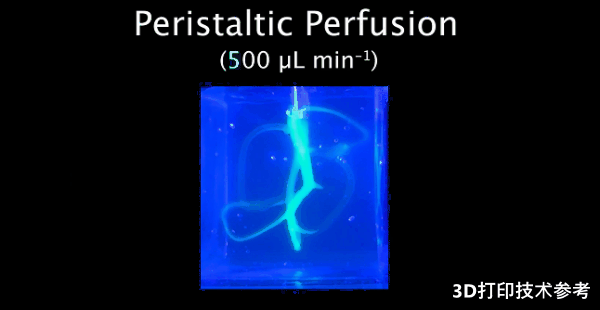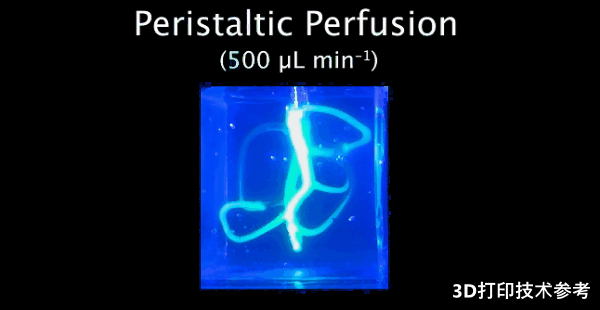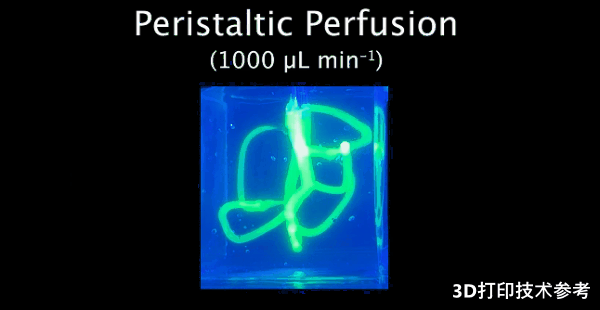 在血管腔的 z 轴方向进行荧光扫描以检测其完整性
在血管腔的 z 轴方向进行荧光扫描以检测其完整性
基于以上方法,设计复杂的血管树需要大量的计算劳动和成本大大降低。相比传统方法的模型设计速度加快了230多倍。
3D打印真实再现功能血管
为了说明组织工程的实用性,研究人员在水凝胶中打印了多种血管结构,水凝胶的自支撑特性使血管打印非常便利。
首先打印的是一个四血管平面网络,确认了防水性和灌注情况。在37°C以上,血管内的支撑材料可融化去除。光学相干断层扫描显示与数字设计相差很小,且受到打印针头和层厚的影响。研究人员还使用染料灌注,验证了管腔的完整性。

为了说明模型驱动的设计血管在组织制造和流动模拟方面的实用性,研究人员在一个立方体组织域中创建了一个非平面的单入口单出口血管网络。在打印前,通过数字孪生网络进行脉动流模拟确认了血流动力学完整性。通过将颗粒墨水挤压到颗粒支撑浴中来制造模型,获得软组织的弹性模量。这种合成血管确保了流量分布均匀,并相应地提高了灌注和存活率。

最后,研究人员利用嵌套3D生物打印技术在两个连续步骤中制造了一个灌注环。打印结构的微型计算机断层扫描(μCT)显示,与数字模型相比,表面偏差很小。
首先在含有高浓度细胞悬浮浴生物墨水中打印出了一个半径为10毫米、高度为18毫米的环形结构(非血管通道)组织。接着,使用基于明胶微颗粒的牺牲生物墨水,在环形结构中打印出由25个相互连接的血管段组成的集成可灌注血管域。作为对照,另一组实验只打印环形结构而不在其中打印血管,该结构在培养基中培养,而前一组则使用灌注形式培养。结果显示,内有血管的环形结构7天后仍然保持高细胞活性,而没有内部血管的机构则活性很低。该实验突出了嵌套式3D生物打印在构建具有可灌注血管域的组织结构方面的优势和应用潜力。

生物打印血管模型的灌注和存活情况
END
在多个尺度上生成定制血管一直是生物打印的重大障碍。在这项工作中,研究人员提出了一种综合的模型驱动管道设计方法,可高效生成任意几何形状的血管网络,结合先进的3D打印技术,将其制造出来。而且,所打印的血管网络能够确保体外的灌注功能和生物相容性。然而,研究也指出,目前大而复杂的具有较小直径血管的血管树仍然难以构建,打印不准确性可能导致灌注的中断或堵塞。
长期来看,组织工程旨在通过患者特定的干预措施替换受损或患病的器官。这项研究仍然扩展了未来合成血管结构在生物制造和患者特定建模中进行更广泛应用的潜在可能性,有望为组织器官再造提供重要的技术支持。






