3D打印最新Science,中国学者团队!
3D打印技术参考注意到,2025年3D打印技术领域第5篇Science文章于5月8日发表。来自发表了题为“Imaging-guided deep tissue in vivo sound printing”的文章。该文章的通讯作者教授,本科就读华中科技大学,硕士毕业于清华大学,现为加州理工学院医学工程教授。
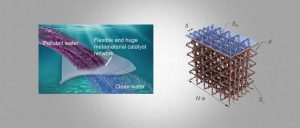
这项研究的重要突破在于,其推出了一个体内3D打印平台,该平台可在实时成像的引导下,使用聚焦超声对活性组织深处的特定位置3D打印生物材料或聚合物。这项工作为组织再生、靶向药物递送、生物电子学和非侵入性治疗开辟了方向。
体内3D打印已成医学研究前沿,超声波技术优势与挑战并存
医学3D打印已经不仅仅局限于从体外制造再赋能医学,3D打印技术参考注意到,深穿透3D打印已成为当前医学工程发展的一个重要方向,其依赖的能量源通常是近外光和超声波。近红外光用于体内3D打印的局限在于穿透力非常有限,只能到达皮下,而超声技术具有深部组织穿透和非侵入性等优势,且具备实时成像能力,可用于精确定位和控制生物材料的原位制造,是当前实现体内3D打印研究的热点,此前哈佛大学也曾将该技术发表在Science上。
本想研究同期评论指出,聚焦超声波可以将高能声波传递到皮肤下深度达20厘米的局部区域,具体取决于超声波的频率和组织的类型。高声学能量还可以与材料相互作用,引发各种化学、物理和生物反应,实现定制化学反应、检测和治疗。但体内的超声3D打印比看起来更加具有挑战性。
利用声波触发化学反应,需要开发声触发墨水,即预聚物的液态配方,但超声波引起振荡气泡和流体运动可能会破坏注入的墨水材料,导致打印速度慢和制造分辨率差。另外,即便可以快速固化,墨水中存在的小反应分子和局部热生成可能会带来生物相容性风险。

超声聚焦+实时成像,实现精准体内3D打印
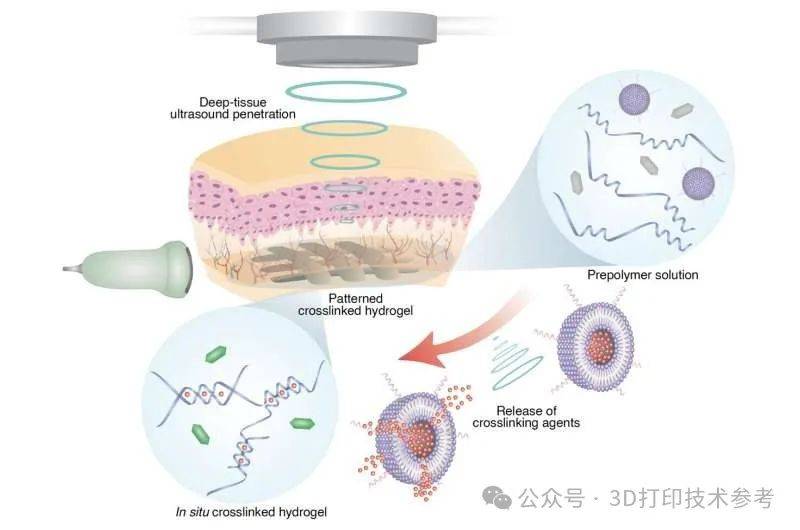
这项研究开发了一种新方法,将超声波与低温敏感脂质体实现结合。这种脂质体是一种球形细胞状囊泡,带有保护性脂肪层,常用于药物输送。在这项研究中,研究人员将交联剂装载到脂质体中,并将其嵌入聚合物溶液中,该溶液包含想要打印的聚合物单体、可以显示交联发生时间的成像造影剂,以及希望输送的物质——如治疗药物。此外,还可以添加其他成分,如细胞和导电材料(碳纳米管或银),然后将复合生物墨水直接注射到体内。
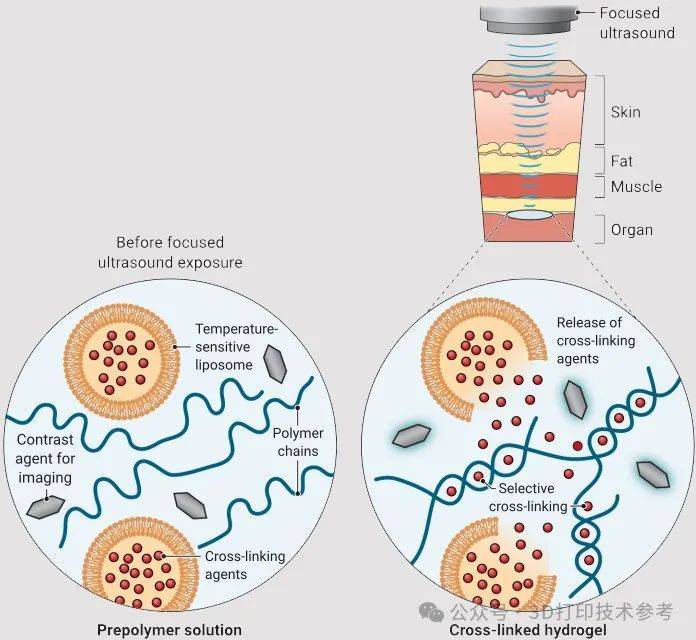
脂质体颗粒对低温敏感,这意味着通过使用聚焦超声波将小目标区域的温度升高约5℃,即可触发有效载荷的释放并启动聚合物的3D打印。具体的说,只需将温度升高几度,脂质体颗粒就能释放交联剂,交联剂释放到哪里,局部聚合或打印就会在哪里发生。
该团队使用源自细菌的气囊作为成像造影剂。这些气囊,即充满空气的蛋白质胶囊,在超声成像中清晰可见,并且对液态单体溶液交联形成凝胶网络时发生的化学变化非常敏感。当这种转变发生时,气囊的对比度实际上会发生变化,可以通过超声成像检测到,这使得科学家能够轻松识别聚合交联发生的时间和精确位置,从而在活体动物体内打印确定的图案。

体内3D打印的治疗效果显著
该团队将这项新技术称为深层组织体内声音打印(DISP)平台。当研究小组使用DISP平台在小鼠膀胱肿瘤附近3D打印载有化疗药物阿霉素的聚合物时,他们发现与通过直接注射药物溶液接受药物的动物相比,几天内肿瘤细胞死亡的数量明显增多,从而证明了该技术在肿瘤治疗中的有效性。
高伟教授表示,他们开发的新技术可以到达深层组织,并能3D打印多种类型的材料,应用广泛,同时能保持优异的生物相容性。该技术依靠声音进行定位,目前已用于3D打印选择性药物输送的聚合物胶囊,以及用于密封内部伤口的胶状聚合物。
除了用于药物和细胞递送的生物粘附凝胶和聚合物外,该研究还描述了该技术在打印生物电水凝胶中的应用。生物电水凝胶是一种嵌入导电材料的聚合物,用于体内监测生理生命体征,例如心电图(ECG)。
总的来说,高伟教授团队开发了一种有效的高精度、可控体内3D打印方法,不仅速度快,而且打印材料具有生物相容性,取得了可观的治疗效果。未来,该团队将在更大的动物模型上进行3D打印,并希望在不久的将来,能够在人体上进行评估。同时还将借助人工智能,希望能够在跳动的心脏等运动器官内自主触发高精度打印。